Carnet de bac
Exercices
Cristal ionique NaCl
| |
| 1) | |||
| On sait que | \(\displaystyle\mathrm{ Na \ K^2 \ L^8 \ M^1 \\ Cl \ K^2 \ L^8 \ M^7 } \) | ||
| donc les atomes de sodium et de chlore possèdent trois couches électroniques. | |||
| D'après la règle de l'octet | \(\displaystyle\mathrm{ Na^+ \ K^2 \ L^8 \\ Cl^- \ K^2 \ L^8 \ M^8 } \) | ||
| donc l'ion sodium possède deux couches alors que l'ion chlorure en possède trois. | |||
2) |
|||
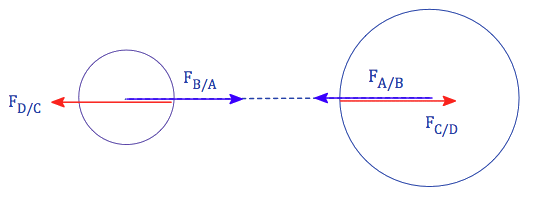
| D'après ce qui précède, l'ion sodium est situé en A alors que l'ion chlorure est situé en B, et | \(\displaystyle\mathrm{ q_A=+e \\ q_B=-e \\ q_C=-e' \\ q_D=-e' } \) | ||
3) |
|||
| D'après la loi de Coulomb | \(\displaystyle\mathrm{ F= K \frac{e^2}{d^2} \\ F'=K \frac{e'^2}{d'^2} } \) | ||
 |
|||
4) |
|||
| D'après la figure | \(\displaystyle\mathrm{ d=d'+r_{Na} +r_{Cl} } \) | ||
5) |
|||
| D'après l'énoncé | \(\displaystyle\mathrm{ F=F' } \) | ||
| donc | \(\displaystyle\mathrm{ K \frac{e^2}{d^2}=K \frac{e'^2}{d'^2} } \) | ||
| soit | \(\displaystyle\mathrm{ d'= d \frac{e'}{e} } \) | ||
| soit | \(\displaystyle\mathrm{ d'= (d'+r_{Na} +r_{Cl} ) \frac{e'}{e} } \) | ||
| soit | \(\displaystyle\mathrm{ d'= (r_{Na} +r_{Cl} ) \frac{e'}{e-e'} } \) | ||
| D'après les données | \(\displaystyle\mathrm{ d'= (181+97) \cdot 10^{-12} \times \frac{1,00 \cdot 10^{-22}}{1,6 \cdot 10^{-19} - 1,00 \cdot 10^{-22}} } \) | ||
| soit | \(\displaystyle \underline{\mathrm{ d'=1,74 \cdot 10^{-13} \ m }} \) | ||
| donc les deux ions sont tangents. | |||