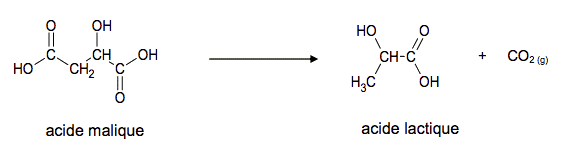|
Après récolte et pressage des raisins, deux fermentations ont lieu, d’abord la fermentation alcoolique, puis la fermentation malolactique. Pour qu’un vin puisse être mis en bouteille, il convient de vérifier que la fermentation malolactique, objet d’étude de cet exercice, est terminée. La fermentation malolactique, généralement assurée par une espèce de bactérie lactique, Oenococcus oeni, désigne la désacidification biologique du vin. Lors de cette transformation, l'acide malique présent dans le vin se transforme en acide lactique, acide plus faible, avec production de dioxyde de carbone à l’état gazeux ; transformation modélisée par la réaction d’équation suivante :
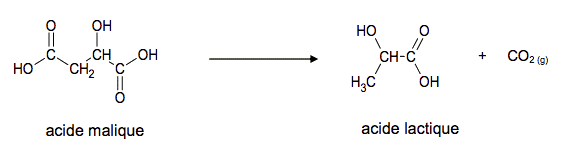
La désacidification du vin qui résulte de la fermentation malolactique est un phénomène généralement recherché, auquel on doit l'assouplissement des vins jeunes.
D’après Vignevin-sudouest et Futura-science
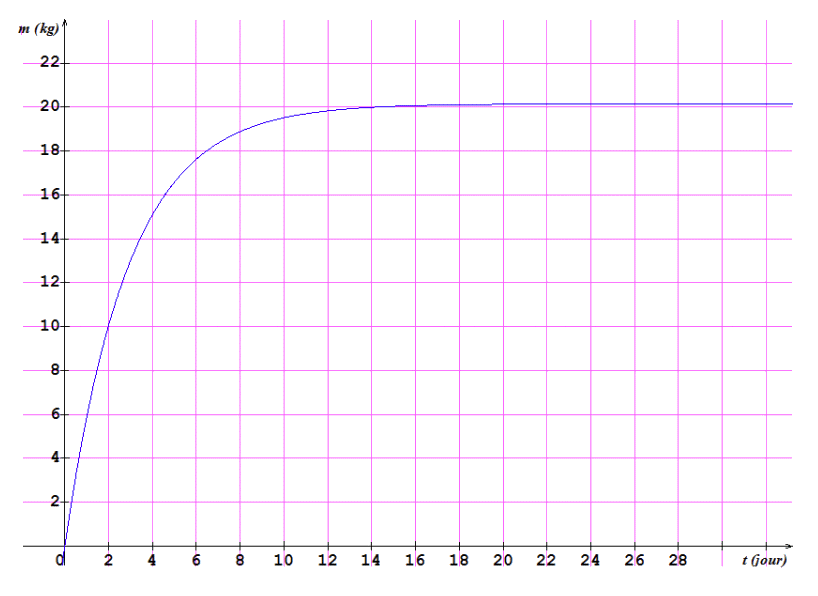
Le 15 octobre 2016, un vigneron suit la fermentation malolactique d’un vin contenu dans une cuve de 10 m3. La température ambiante est de 15 °C lorsque la fermentation malolactique débute. La concentration massique initiale en acide malique dans le vin est de 3,0 g·L-1. L’évolution au cours du temps de la masse d’acide lactique formé est donnée par le graphique situé en annexe, à rendre avec la copie.
Données :
- masse molaire de l'acide malique : Mmal = 134,0 g·mol-1
- masse molaire de l'acide lactique : Mlac = 90,0 g·mol-1
- pour simplifier les écritures, on notera les couples acidobasiques
- de l’acide malique : AH2 / AH- : pKA1 = 3,46 ; AH- /A2- : pKA2 = 5,10
- de l’acide lactique : A'H/ A'- : pKA = 3,86
1. Stéréochimie
1.1. Réécrire l'équation de la réaction chimique modélisant la transformation de l'acide malique en acide lactique en utilisant les formules topologiques des molécules.
1.2. Entourer et nommer les groupes caractéristiques présents dans la molécule d'acide malique.
1.3. À l’aide de la représentation de Cram, dessiner les stéréoisomères de la molécule d’acide lactique.
2. Acidité et vin
L'acide malique est un diacide. Il peut apparaître sous différentes formes en fonction du pH de la solution.
2.1. Définir la notion d'acide. Justifier alors la notation AH2 utilisée pour l’acide malique.
2.2. Représenter les domaines de prédominance, en fonction du pH, des différentes formes de l acide malique et de l’acide lactique en utilisant les notations simplifiées indiquées dans les données.
2.3. La concentration en ions oxonium H3O+ dans le vin, en début de fermentation malolactique, est de 6,3·10– 4 mol·L-1. Calculer la valeur du pH du vin en début de fermentation.
2.4. En déduire la forme prédominante de l'acide malique dans le vin en début de fermentation malolactique.
2.5. Proposer des éléments d’interprétation à « la désacidification résultant de la fermentation malolactique» indiquée dans le texte d’introduction.
3. Suivi de la fermentation malolactique
3.1. Montrer que la quantité de matière initiale en acide malique dans la cuve est de 2,2·102 mol.
3.2. En s’appuyant sur le graphique situé en annexe, déterminer la quantité de matière d’acide lactique formé à l’état final.
3.3. La fermentation malolactique est-elle une transformation chimique totale ? Justifier.
3.4. Définir le temps de demi-réaction d'une transformation chimique.
3.5. Montrer que la masse d’acide lactique formé est proportionnelle à l’avancement de la réaction. Déterminer graphiquement le temps de demi-réaction pour cette fermentation malolactique. On fera apparaître la méthode utilisée sur le graphique situé en annexe, à rendre avec la copie.
3.6. À partir de quelle date le viticulteur pourra-t-il mettre en bouteille le vin de ses cuves ? Justifier.
3.7. Représenter sur le graphique situé en annexe, à rendre avec la copie l’allure quantitative de la courbe de suivi de la fermentation malolactique si la température ambiante est de 20 °C. Justifier. En déduire l’influence de cette nouvelle condition sur la mise en bouteille.
4. Chromatographie sur couche mince d’un vin à mettre en bouteille
Le viticulteur souhaite mettre le vin d’une cuve en bouteille. Il effectue une chromatographie de contrôle de la fermentation malolactique sur un échantillon de vin de la cuve. Les résultats sont présentés ci-dessous :

Dépôt 1 : acide lactique
Dépôt 2 : acide malique
Dépôt 3 : vin à mettre en bouteille
4.1. Le viticulteur peut-il mettre ce vin en bouteille ? Justifier.
4.2. Quel(s) problème(s) veut-on éviter en suivant l’évolution de la fermentation malolactique dans les vins avant la mise en bouteille ?
5. Spectroscopie RMN du proton et fermentation malolactique
5.1. Parmi les spectres simulés ci-après, lequel pourrait correspondre à l'acide lactique ? Expliciter la démarche mise en œuvre et attribuer rigoureusement les signaux correspondants.
Spectres RMN simulés de l’acide malique et de l’acide lactique
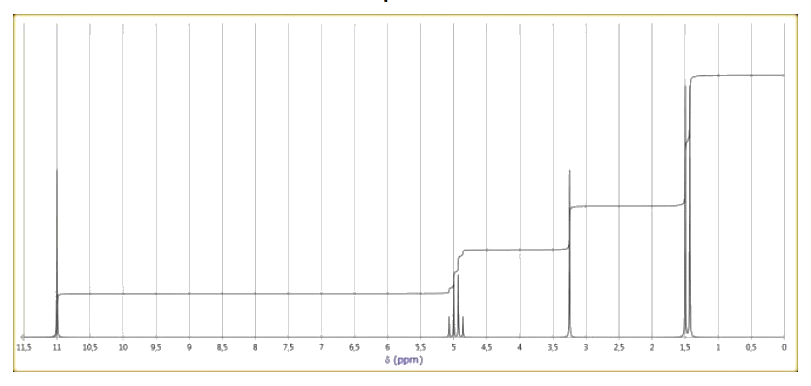
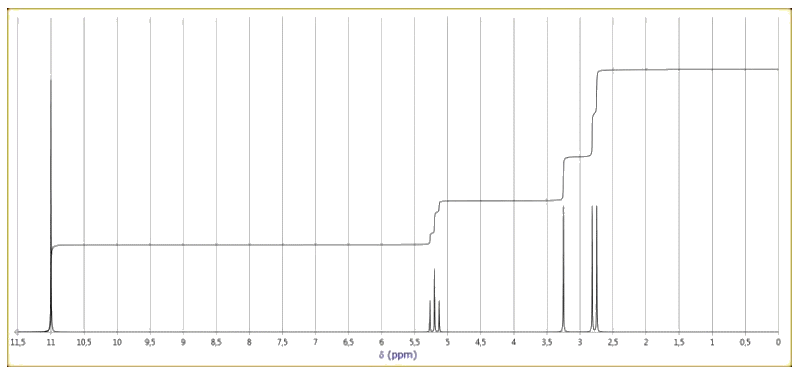
5.2. La spectroscopie RMN pourrait-elle être utilisée pour affirmer que la fermentation malolactique est terminée ? Justifier.
|