|
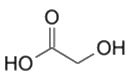
L'acide glycolique est le plus petit des acides α-hydroxylés, il sera noté AH. L'acide glycolique peut être obtenu à partir d'extrait de canne à sucre, de betterave ou de raisin. Grâce à son excellente capacité à pénétrer la peau, l'acide glycolique est très utilisé dans les produits de soins pour la peau, le plus souvent dans les peelings (technique destinée à régénérer la peau du visage). L'acide glycolique permet d'améliorer la texture et l'apparence de la peau. Il peut réduire les rides, l'acné ou l'hyperpigmentation.
D’après Wikipédia
Données à 25°C :
Acide glycolique :
- très bonne solubilité dans l’eau ;
- masse volumique : 1,49 g·cm-3 ;
- masse molaire : 76 g·mol-1 ;
- pKa (acide glycolique / ion glycolate) = 3,83.
Table simplifiée de données pour la spectroscopie IR
| Liaison | Nombre d’onde (cm-1) |
| O-H | alcool 3200-3400 |
| N-H | amine 3100-3500 |
| Ctri-H | 3000-3100 |
| Ctét-H | 2800-3000 |
| O-H acide carboxylique | 2500-3200 |
| C=O ester | 1700-1740 |
| C=O aldéhyde ou cétone | 1650-1730 |
| C=O acide carboxylique | 1680-1710 |
| N-H amine ou amide | 1560-1640 |
Les trois parties de l’exercice sont indépendantes.
Partie A : étude de l’acide glycolique
1. En nomenclature officielle, l’acide glycolique s’appelle l’acide hydroxyéthanoïque. Justifier le nom officiel de cet acide.
2. L’acide glycolique possède-t-il des stéréoisomères de configuration ? Justifier. La canne à sucre subit deux broyages donnant un liquide sucré appelé le « vesou ». Celui-ci contient des acides organiques dont l’acide glycolique.
3. Une chromatographie révélée par le bleu de bromophénol permet de vérifier que le « vesou » contient bien de l’acide glycolique.
| Forme acide | Forme basique | Zone de virage |
| Bleu de bromophénol | Jaune | Bleu | 3,0 - 4,6 |

L’éluant, de pH = 2, est un mélange de :
- 70% de butan-1-ol ;
- 30% de solution concentrée d’acide éthanoïque ;
- Quelques gouttes de solution à 1 g·L-1 de bleu de bromophénol.
Nature des dépôts :
- dépôt 1 : vesou ;
- dépôt 2 : acide glycolique pur.
Lors du séchage de la plaque de chromatographie (photo ci-contre), l’acide éthanoïque s’évapore. Après séchage, le chromatogramme, reproduit ici en noir et blanc, présente en réalité des taches jaunes sur fond bleu.
3.1. Quelle est la couleur de l’éluant ?
3.2. Proposer une explication des couleurs des taches observées sur le chromatogramme après séchage et interpréter le chromatogramme.
4. En supposant que la teneur en masse d’acide glycolique dans la matière organique extraite du « vesou » est de 0,1%, quelle masse de « vesou » serait nécessaire pour obtenir 100 mL d’acide glycolique pur ?
5. Dans l'industrie, l'acide glycolique n'est pas extrait de la canne à sucre mais synthétisé à partir du glyoxal, selon une réaction de Cannizzaro d’équation suivante :

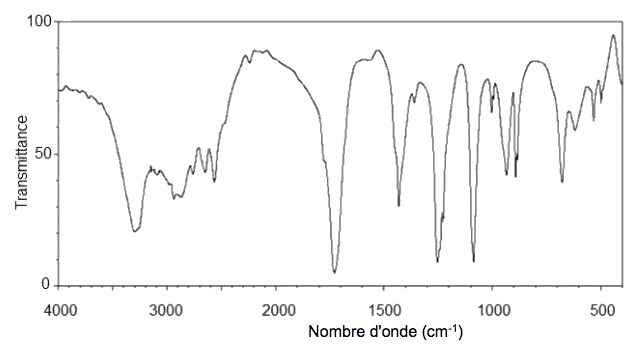
Un spectre infrarouge du produit finalement obtenu est donné ci-après. Avancer deux arguments pour justifier qu’il peut correspondre à l’acide glycolique.
Partie B : étude d’une solution dermatologique d’acide glycolique
En dermatologie, il existe plusieurs solutions aqueuses, de concentrations différentes en acide glycolique, utilisées dans le traitement de l’acné : 20% ; 35% ; 50% ou 70% en masse d’acide glycolique.
Pour rédiger l’étiquette d’une solution d’acide glycolique en dermatologie, on se propose d’en déterminer les caractéristiques : masse volumique et pourcentage massique d’acide glycolique.
1. Proposer une méthode pour déterminer expérimentalement la masse volumique de la solution d’acide glycolique. Sachant que la solution a une masse volumique ρ = 1,26 g·cm-3, indiquer le matériel utilisé, les valeurs des prélèvements et les mesures correspondant à la méthode choisie.
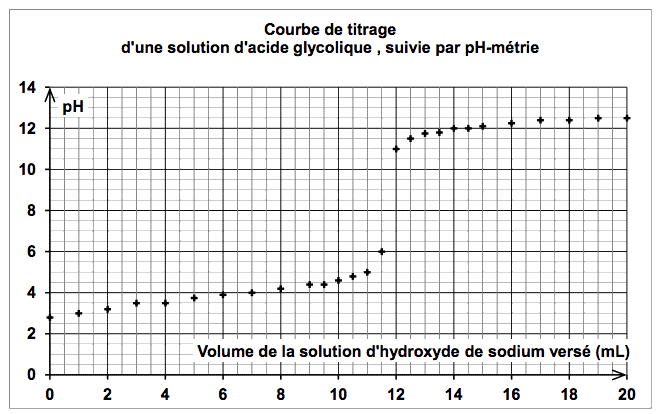
2. Pour déterminer le pourcentage massique d’acide glycolique, on réalise le titrage décrit ci-dessous dans ses grandes lignes. On dispose de 50 mL d’une solution d’acide glycolique que l’on dilue vingt fois. On réalise le titrage suivi par pH-métrie d’une prise d’essai de 10,0 mL de la solution
diluée par une solution aqueuse d’hydroxyde de sodium, (Na+(aq) + HO−(aq)), de concentration molaire égale à 5,0·10−1 mol·L−1. On obtient les résultats expérimentaux suivants.
2.1 Décrire la préparation de 100,0 mL de solution dermatologique diluée 20 fois.
2.2 Réaliser un schéma annoté du montage permettant d’effectuer le titrage. Le diagramme de distribution des espèces du couple acide glycolique / ion glycolate représenté ci-dessous donne le pourcentage de chaque forme en fonction du pH.

2.3. Identifier, sur le diagramme de distribution, la courbe correspondant à l’acide glycolique (AH) et celle correspondant à l’ion glycolate A. Justifier.
2.4 Quelle est la forme prédominante du couple acide glycolique / ion glycolate (AH / A-) au début du titrage ? Puis à la fin du titrage ? Justifier.
2.5 En déduire l’équation chimique de la réaction support du titrage.
2.6 Quel pourcentage massique d’acide glycolique doit être indiqué sur l’étiquette ?
Le candidat est invité à prendre des initiatives et à présenter la démarche suivie même si elle n’a pas abouti.
Partie C : l’acide polyglycolique pour les sutures internes
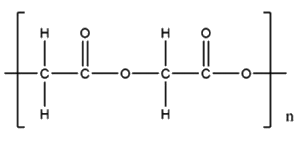
L’acide glycolique est également à la base de la fabrication d’un polymère biodégradable, l’acide polyglycolique, noté PGA (formule cicontre), utilisé en chirurgie depuis 1970 pour réaliser des sutures internes résorbables. Le caractère résorbable ou non d’un fil est défini par sa vitesse de perte de résistance. La résorption du PGA se fait par l’action de l’eau des tissus qui hydrolyse des fonctions du polymère ; les produits de l’hydrolyse sont ensuite éliminés naturellement par les fluides biologiques de l’organisme.
1. Identifier et reproduire le groupe caractéristique présent dans l’acide polyglycolique.
2. L’hydrolyse d’un ester correspond à la réaction de cet ester avec de l’eau pour former un acide carboxylique et un alcool ; cette transformation est lente à température ambiante. Proposer une interprétation à la résorption du PGA sous l’action de l’eau contenue dans les tissus.
L’abécédaire des sutures B. Braun fournit les informations suivantes.
- Evolutions temporelles de la résistance des sutures à la traction et de la résistance des tissus lors de la cicatrisation de la plaie (ces deux évolutions ne sont pas linéaires : le graphe ci-dessous donne seulement la tendance).

Délai de cicatrisation en fonction des tissus
| Tissu | Délai de cicatrisation |
| Tissu sous cutanés | 2 semaines |
| Intestin | 2 à 3 semaines |
| Vessie | 5 jours 75 à 90 % de sa résistance initiale retrouvée en 2 semaines |
| Ligaments/tendons | 6 semaines 50 à 70 % de sa résistance initiale retrouvée après 1 an |
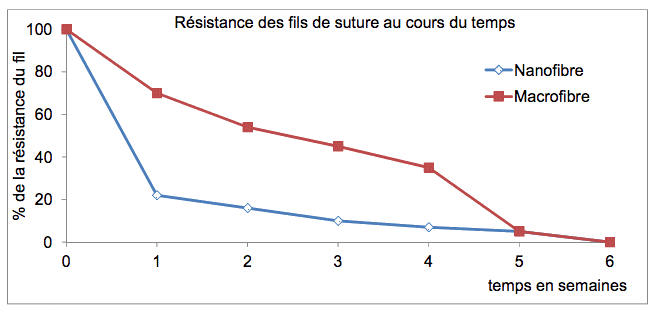
3. Un chirurgien souhaite effectuer la suture d’un intestin. Parmi les deux fils de suture proposés (nanofibre ou macrofibre), lequel est le plus adapté ?
La démarche nécessite d’être correctement présentée.
|