Carnet de bac
Annales
Du lait au yaourt |
➔ |
| Liban 2014 - Exercice 1 - 6 points |
| 1.1) | |||
| D'après les définitions des groupes hydroxyle et carboxyle, la molécule d'acide lactique contient un groupe hydroxyle entouré en vert, et un groupe carboxyle entouré en bleu (pointillets). | 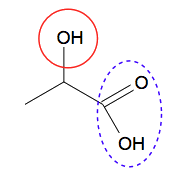 |
||
1.2.) |
|||
| D'après la formule de la molécule, elle contient un carbone asymétrique donc elle est chirale et possède un énantiomère | |||
 |
|||
1.3.1) |
|||
| Si l'acide lactique est un acide fort alors | \(\displaystyle\mathrm{ pH=-log \ c } \) | ||
| D'après les données | \(\displaystyle\mathrm{ pH=-log \ (1,5 \cdot 10^{-3} } \) | ||
| donc | \(\displaystyle\mathrm{ pH=2,9 } \) | ||
| D'après l'énoncé la valeur du pH est de 3,4 donc l'acide lactique n'est pas un acide fort. | |||
1.3.2) |
|||
| Si pH>pKa alors c'est l'espèce basique qui prédonmine. | |||
| D'après l'énoncé la valeur du pH est supéireure à celle du pKa donc c'est l'ion lactate qui prédomine. | |||
2.1) |
|||
| On sait que la phénolphtaléine est de couleur rose en milieu basique et incolore en milieu acide. | |||
| On sait que la valeur du pH est brutalement modifée autour de l'équivalence. | |||
| donc la persitance de la couleur rose indique l'équivalence. | |||
2.2) |
|||
On note
|
|||
| D'après la définition du degré Dornic | \(\displaystyle\mathrm{ Δ = 10 \frac{m}{V_{lait}} } \) | ||
On note
|
|||
| D'après la définition de la concentration molaire | \(\displaystyle\mathrm{ c= \frac{n_b}{V_b} } \) | ||
| D'après la définition de la masse molaire | \(\displaystyle\mathrm{ M = \frac{m}{n_a} } \) | ||
| On sait qu'à l'équivalence | \(\displaystyle\mathrm{ n_a=n_b } \) | ||
| donc | \(\displaystyle\mathrm{ Δ = 10 \frac{M \ c_b \ V_E}{V_{lait}} } \) | ||
| D'après les données | \(\displaystyle\mathrm{ Δ = 10 \frac{90 \times 0,11 \times 1,4 \cdot 10^{-3}}{10 \cdot 10^{-3}} } \) | ||
| soit | \(\displaystyle \underline{\mathrm{ Δ = 14°D }} \) | ||
| D'après l'énoncé un lait est frais si son degré Dornic est inférieur à 18, ce qui est le cas, donc ce lait est frais. | |||
2.3) |
|||
| D'après l'énoncé le volume versé est de 1,4mL ce qui est très faible. Il serait plus judicieux d'utiliser une solution titrante moins concentrée pour obtenir un volume à l'équivalence plus grand et donc une erreur relative sur ce volume plus faible. Par exemple, la solution pourrait être diluée 10 fois, ce qui donnerait un volume à l'équivalence de 14mL, de cette manière, le volume versé donnerait aussi la valeur du degré Dornic. | |||
3) |
|||
| D'après le document 3 l'acidité doit être forte et d'après le document 4 la température donnant la plus forte acidité rapidement est θ3=45°. | |||
| D'après le document 5 le pH doit être inférieur à 4,6 et d'après le document 6 cette condition est réalisée à partir d'une durée de 6h. | |||