Carnet de bac
Annales
Le diester |
➔ |
| Pondichéry 2016 - Exercice 1 - 4 points |
| 1) | |||
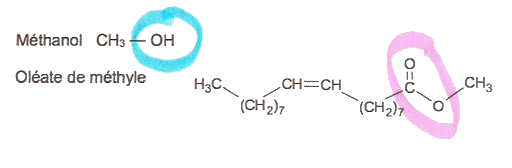
| D'après le schéma ci-dessous, la fonction entourée en bleu est un groupe hydroxyle et la fonction entourée en rose est un groupe ester. | |||
 |
|||
2) |
|||
| D'après sa formule, la glycérine porte trois groupes hydroxyle et trois atomes de carbone sur la principale chaîne carbonnée, donc la molécule est propan-1,2,3-triol. | |||
3) |
|||
| D'après les sites donneurs et accepteurs présents : | |||
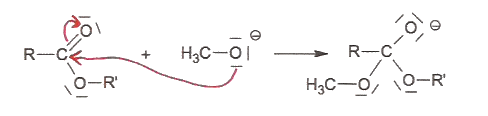 |
|||
4) |
|||
| D'après les différentes étapes de la réaction, l'hydroxyde est consommé et régénéré en fin de réaction, c'est donc un catalyseur basique. | |||
5) |
|||
| D'après les données, l'indice cétane du Diester est beaucoup plus proche de celui du gazole que celui de l'huile de colza. | |||
6) |
|||
On note
|
|||
| D'après la définition de la masse molaire | \(\displaystyle\mathrm{ n_c = \frac{m_c}{M_c} \\ n_d = \frac{m_d}{M_d} } \) | ||
| D'après la définition de la masse volumique | \(\displaystyle\mathrm{ ρ = \frac{m_d}{V_d} } \) | ||
| D'après la stœchiométrie de la réaction, | \(\displaystyle\mathrm{ r= \frac{n_d}{3 \ n_c} } \) | ||
| donc | \(\displaystyle\mathrm{ r= \frac{ρ \ V_d \ M_c}{3 \ M_d \ m } } \) | ||
| D'après les données | \(\displaystyle\mathrm{ r= \frac{880 \times 1200 \times 0,884}{3 \times 296 \times 1150 } } \) | ||
| soit | \(\displaystyle\mathrm{ r= 91 \% } \) | ||
| donc la réaction n'est pas totale, son rendement est de 91% seulement. | |||
7) |
|||
| D'après les données du texte, l'ajout d'agrocarburant dans le gazole présente un bilan carbone intéressant mais sa production nécessite l'occupation de terres cultivables. | |||