|

Le sucre produit dans les feuilles de betteraves sucrières grâce à la photosynthèse s'accumule dans la racine sous forme de saccharose. Le bioéthanol - éthanol issu de l’agriculture - peut notamment être obtenu par fermentation du sucre extrait des racines de betterave sucrière. Le bioéthanol peut être incorporé à l’essence utilisée par un grand nombre de moteurs de voiture.
Dans cet exercice, on s’intéresse au saccharose présent dans la betterave sucrière, à la production d’éthanol par fermentation du saccharose et à l’utilisation du bioéthanol dans les carburants.
Données :
- Economie betteravière en France pour la récolte 2009 :
- rendement de la culture de betterave sucrière : 74,8 tonnes par hectare
- pourcentage massique moyen de saccharose dans la betterave : 19,5 %
- Surface agricole française cultivée : environ 10 millions d’hectares
- Masse volumique de l’éthanol : ρ = 789·103g·m-3
- Masses molaires moléculaires : M (éthanol) = 46,0 g·mol-1 ; M (saccharose) = 342,0 g·mol-1
- Electronégativités comparées χ de quelques éléments : χ(O) > χ(C), χ(C) environ égale à χ(H)
- Données de spectroscopie infrarouge :
| Liaison |
O – H libre |
O – H lié |
N – H |
C – H |
C = O |
C = C |
Nombre d’onde
σ (en cm-1) |
3600
Bande fine |
3200 - 3400
Bande large |
3100-3500 |
2700-3100 |
1650-1750 |
1625-1685 |
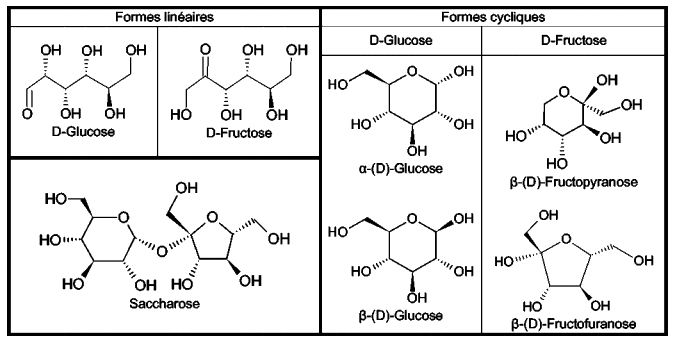
- Formules topologiques de quelques sucres :
1. Étude de la structure du saccharose
Le saccharose est formé à partir du D-Glucose et du D-Fructose.
1.1. Écrire la formule développée de la forme linéaire du D-Glucose, puis identifier par un astérisque les atomes de carbone asymétriques.
Par réaction entre deux de ses groupes caractéristiques, la forme linéaire du D-Glucose peut se transformer en l’une ou l’autre de ses formes cycliques lors d’une réaction de cyclisation. En solution aqueuse à 25°C, il s’établit un équilibre entre les différentes formes du glucose avec les proportions suivantes : 65 % de β-(D)-Glucose, 35 % de α-(D)-Glucose et environ 0,01 % de forme linéaire de D-Glucose. Le mécanisme de la cyclisation est proposé ci-dessous, il peut conduire à l’un ou l’autre des stéréoisomères cycliques.
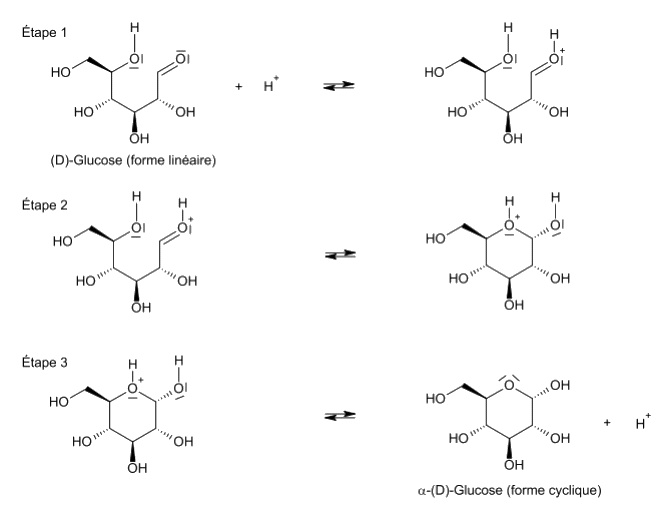
1.2. Dans un mécanisme réactionnel apparaissent usuellement des flèches courbes; que représentent-elles ? Compléter les trois étapes du mécanisme de cyclisation du D-Glucose figurant en annexe avec les flèches courbes nécessaires.
1.3. Le spectre infrarouge obtenu par analyse d’un échantillon de glucose est fourni ci-dessous. Ce spectre confirme-t-il la très faible proportion de la forme linéaire dans le glucose ? Justifier.
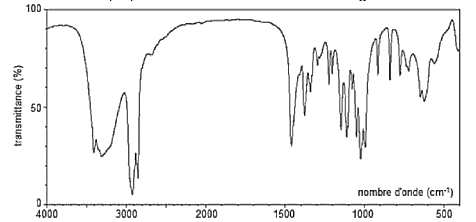
Source : National Institute of Advanced Industrial Science and Technology
1.4. Les formes linéaires du D-Glucose et du D-Fructose sont-elles stéréoisomères ? Justifier.
1.5. À partir de quelles formes cycliques du D-Glucose et du D-Fructose le saccharose est-il formé ?
Le saccharose contenu dans 30 g de betterave sucrière est extrait avec de l’eau grâce à un montage à reflux. À la fin de l’extraction, on recueille une solution aqueuse S qui contient 5,8 g de saccharose.
1.6. L’eau est un solvant adapté à cette extraction. Proposer une explication à la grande solubilité du saccharose dans ce solvant.
On hydrolyse ensuite, en milieu acide, le saccharose contenu dans la solution S. L’hydrolyse peut être modélisée par une réaction d’équation :
| C12H22O11 (aq) |
+ |
H2O (ℓ) |
→ |
C6H12O6 (aq) |
+ |
C6H12O6 (aq) |
| Saccharose |
|
Eau |
|
Glucose |
|
Fructose |
On suppose que la transformation est totale, que l’eau est en excès et qu’initialement la betterave ne contenait ni glucose ni fructose.
1.7. Émettre une hypothèse sur le rôle de l’acide utilisé lors de cette hydrolyse et proposer une expérience simple permettant de la tester.
On a réalisé la chromatographie du saccharose, du D-Glucose et du D-fructose. Le chromatogramme obtenu est donné et schématisé en annexe. Tous les chromatogrammes de l'annexe sont supposés réalisés dans les mêmes conditions expérimentales que celui qui est photographié.
1.8. Représenter sur l'annexe l’allure du chromatogramme obtenu après élution et révélation, sachant que :
- le dépôt A est un échantillon du milieu réactionnel avant hydrolyse du saccharose ;
- le dépôt B est un échantillon du milieu réactionnel au cours de l’hydrolyse du saccharose ;
- le dépôt C est un échantillon du milieu réactionnel après hydrolyse complète du saccharose.
2. Du saccharose au bioéthanol
La fermentation alcoolique des jus sucrés sous l'action de micro-organismes est une source de production d'alcools. Dans le cas de la betterave sucrière, la solution de saccharose (jus sucré) extrait de la betterave fermente pour produire de l’éthanol (bioéthanol) et du dioxyde de carbone selon la réaction supposée totale d’équation :
| C12H22O11 (aq) | + | H2O (ℓ) | → | 4 C2H6O (aq) | + | 4 CO2 (aq) |
2.1. Écrire la formule semi-développée de l’éthanol.
2.2. Attribuer à la molécule d’éthanol l’un des deux spectres de RMN proposés ci-dessous. Justifier.
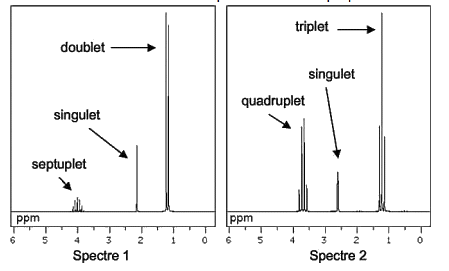
Source : National Institute of Advanced Industrial Science and Technology
2.3. Déterminer la masse d’éthanol obtenu par la fermentation du saccharose contenu dans une betterave sucrière de masse 1,25 kg.
3. Et si on roulait tous au biocarburant ?

L’objectif de cette partie est de déterminer la surface agricole à mettre en culture avec de la betterave sucrière pour que la France devienne autosuffisante en bioéthanol. On fait l’hypothèse que la totalité du parc automobile utilise du carburant contenant du bioéthanol obtenu à partir du saccharose extrait de la betterave. Dans cette hypothèse, on estime que le volume de bioéthanol nécessaire au fonctionnement du parc automobile pendant un an est de l’ordre de 3·106 m3.
Montrer que la masse de betteraves sucrières qu’il faut pour produire ce volume de bioéthanol est de l’ordre de 2·107 tonnes. En déduire l’ordre de grandeur de la surface agricole nécessaire à cette production de betteraves sucrières. Comparer avec la surface agricole française cultivée de 2009.
Le candidat est invité à prendre des initiatives et à présenter la démarche suivie, même si elle n’a pas abouti. La démarche est évaluée et nécessite d’être correctement présentée.
|