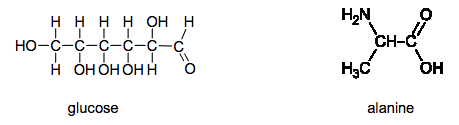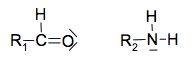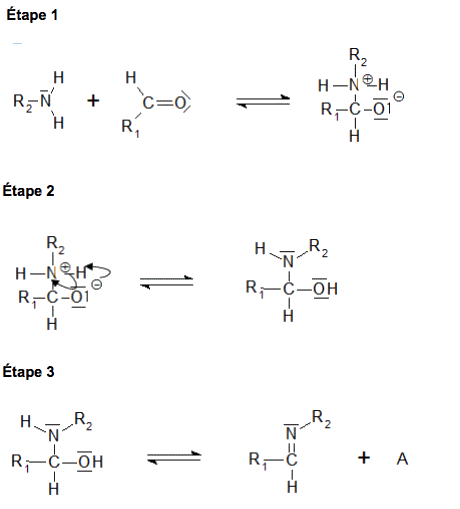|
Louis Maillard rend publique sa découverte fortuite le 27 novembre 1911, dans une communication : « L'action des sucres sur les acides aminés ». La « réaction » qu’il y décrit fait intervenir une succession de transformations chimiques au cours desquelles réagissent des acides aminés avec des sucres réducteurs pour conduire à la formation de mélanoïdines insolubles, composés de couleur caractéristique jaune-orangé, et à d’autres produits volatils et odorants. Cette « réaction » se produit dans presque toutes les préparations culinaires, en particulier pendant la cuisson des viandes. Plus la coloration des mélanoïdines est importante, plus le processus est avancé. Le but de l’exercice est de montrer comment la connaissance et le contrôle de la « réaction » de Maillard permettent d’agir sur le goût et l’aspect d’un aliment.
Données :
- Electronégativité (échelle de Pauling) de quelques éléments chimiques : H : 2,2 ; C : 2,6 ; N : 3,0 ; O : 3,4 ;
- Masse molaire moléculaire : Mglucose=180 g·mol-1 ; Malanine=89 g·mol-1 ;
- Masse volumique de l’eau : ρ = 1,0 g·mL-1 ;
- Arômes générés par la « réaction » de Maillard, en fonction des conditions expérimentales :
| Acide aminé | Sucre | Arôme ou goût généré à 100°C | Arôme ou goût généré à 180°C |
| Cystéine | ribose | bœuf
rôti | |
| Lysine | glucose | pain (pH = 5,2)
tisane (pH = 1) | |
| Valine | glucose | pain de seigle | chocolat fort |
| Alanine | glucose | caramel | sucre brûlé |
| Méthionine | glucose | pomme de terre (pH = 5,2)
viande (pH = 1) | |
| Phénylalanine | glucose | rose | violette |
Partie I : Étude de la « réaction » de Maillard
1. Les réactifs
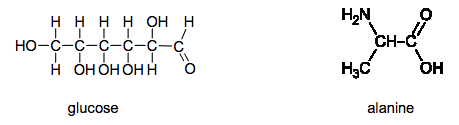
1.1. Justifier que l’alanine soit un acide aminé.
1.2. Justifier le fait que l’alanine possède des stéréoisomères. Donner une représentation de Cram de chacun de ces stéréoisomères. Préciser le type de relation, énantiomérie ou diastéréoisomérie, entre ces stéréoisoméres.
2. Mécanisme d’une partie de la « réaction » de Maillard
Un des mécanismes proposé pour la « réaction » de Maillard fait intervenir trois étapes représentées figure 1. Les molécules de glucose et d’alanine sont respectivement représentées par les formules simplifiées suivantes :
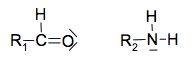
Figure 1
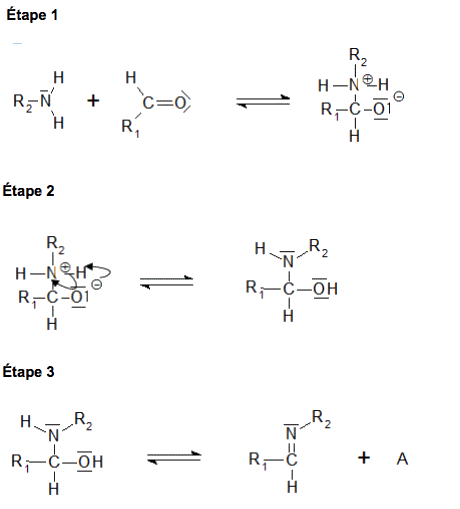
2.1. Identifier, en justifiant votre réponse, les sites donneurs et accepteurs de doublets d'électrons présents dans les molécules de glucose et d’alanine représentées dans le mécanisme.
2.2. Recopier et compléter les étapes 1 et 3 avec une ou plusieurs flèches courbes pour rendre compte de ces étapes.
2.3. Donner la formule de l’espèce chimique A intervenant dans l’étape 3.
Partie II : Suivi de la « réaction » de Maillard
Dans le but d’étudier et d’optimiser la « réaction » de Maillard, on effectue un suivi en laboratoire de la réaction conduisant aux mélanoïdines afin de déterminer les facteurs qui influencent sa cinétique.
Étude expérimentale
Produits, solutions :
- glucose solide ; alanine solide ;
- solution tampon phosphate : pH = 7,8 ;
- solution tampon acétique pH = 4,8 ;
- solution de glucose de concentration molaire c, dans chacune des solutions tampon ;
- solution d’alanine de concentration molaire c, dans chacune des solutions tampon.
Lors des expériences, plusieurs tubes à essais fermés contenant un mélange équimolaire (solide ou en solution) de glucose et d’alanine ont été préparés et placés dans un bain-marie. Différents paramètres ont été modifiés ou différentes substances ont été ajoutées, en fonction du facteur à tester.
Pour suivre l’évolution de la « réaction » de Maillard, une fois le tube à essais sorti de l’eau du bain-marie, on le plonge dans un bain eau - glace. On introduit ensuite une partie du mélange dans la cuve d’un spectrophotomètre réglé sur une longueur d’onde de 420 nm. On relève l’absorbance A du mélange. Les résultats obtenus pour chaque expérience sont retranscrits ci-dessous sous forme de graphiques :
Expérience 1 : mélange équimolaire de glucose et d’alanine dans une solution tampon phosphate, 80 min de chauffage à différentes températures.
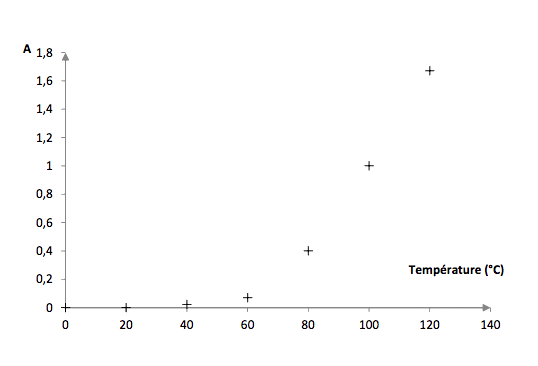
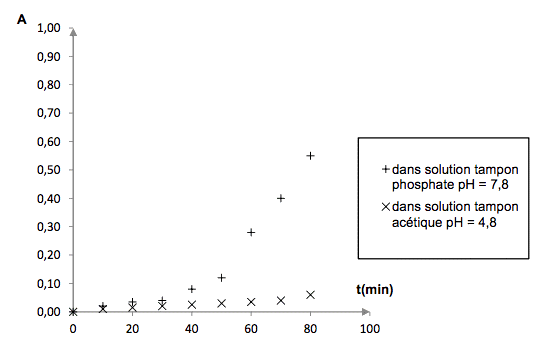
Expérience 2 : mélange équimolaire de glucose et d’alanine à la température 80°C.
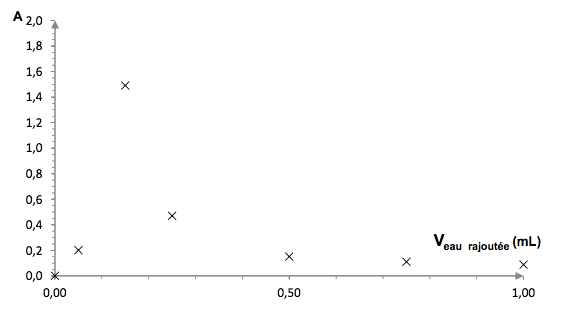
Expérience 3 : mélange équimolaire à 2,0·10-3 mol de glucose solide et d’alanine solide dissous dans différents volumes d’eau (Veau rajoutée ), 80 min de chauffage à la température de 80°C.
1. Avant chaque analyse, les tubes à essais sont plongés dans un bain eau - glace. Quel est le rôle de cette opération ?
2. Justifier qualitativement le fait que des mesures d’absorbance permettent de suivre l’évolution de la « réaction » de Maillard.
3. À l’aide des résultats expérimentaux, et en justifiant les réponses, déterminer les facteurs qui influent sur la « réaction » de Maillard et décrire leurs actions.
4. Déterminer les masses des réactifs et d’eau à prélever pour réaliser le mélange équimolaire et avoir une réaction optimale à 80°C. Déterminer le pourcentage massique d’eau.
5. À l'aide du mécanisme réactionnel, expliquer pourquoi la « réaction » de Maillard est favorisée par un pH supérieur à 11. On pourra s’aider d’un diagramme de prédominance.
Partie III : Conclusion
En quoi la « réaction » de Maillard permet d’expliquer qu’un aliment doré à la poêle n’a pas le même aspect ni le même goût que le même aliment cuisiné à la vapeur ? Vous vous baserez sur les différentes informations fournies et sur les conclusions apportées précédemment pour argumenter vos réponses.
|