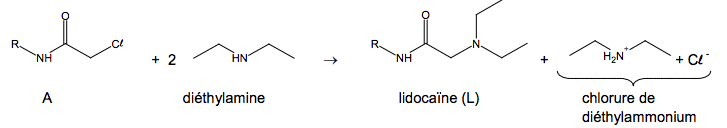Carnet de bac
Annales
Crème anesthésiante |
|
| Métropole 2018 - Exercice 3 - 5 points |
|
Certains actes médicaux sont douloureux ; le confort du patient peut être amélioré par une anesthésie locale.
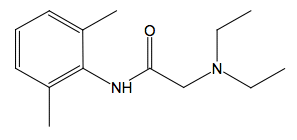
1. Étude de la molécule de lidocaïne
D’après National Institute of Advance Industrial Science and Technology
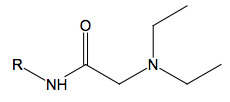
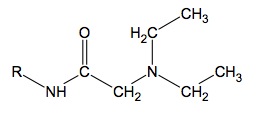
1.2. Recopier, sur la copie, la formule semi-développée simplifiée de la molécule de lidocaïne (formule 3). Identifier sur cette formule le(s) groupe(s) de protons équivalents correspondant au quadruplet situé à 2,7 ppm et ceux correspondant au triplet situé à 1,1 ppm sur le spectre de RMN. Justifier.
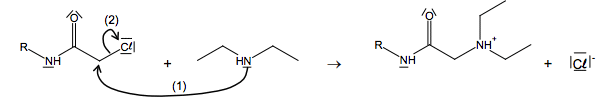
2. Synthèse de la lidocaïne L’équation de la réaction de synthèse de la lidocaïne est la suivante :
|
||||||||||||||