Carnet de bac
Annales
Le génie des physiciens et des chimistes au service de la mesure du temps |
|
| Afrique 2013 - Exercice 3 - 5 points |
|
La mesure du temps est une question essentielle depuis... la nuit des temps. Elle a initialement été basée sur l’observation d’un phénomène régulier et répétitif qui permettait de caractériser des durées égales.
|
|
Document 1
« J’ai pris deux boules, l’une de plomb et l’autre de liège, celle-là au moins cent fois plus lourde que celle-ci, puis j’ai attaché chacune d’elles à deux fils très fins, longs tous les deux de quatre coudées ; les écartant alors de la position perpendiculaire, je les lâchais en même temps ; une bonne centaine d’allées et venues, accomplies par les boules elles-mêmes, m’ont clairement montré qu’entre la période du corps pesant et celle du corps léger, la coïncidence est telle que sur mille vibrations comme sur cent, le premier n’acquiert sur le second aucune avance, fût-ce la plus minime, mais que tous les deux ont un rythme de mouvement rigoureusement identique. On observe également l’action du milieu qui, en gênant le mouvement, ralentit bien davantage les vibrations du liège que celles du plomb, sans toutefois modifier leur fréquence. D’après Discours et démonstrations mathématiques concernant deux sciences nouvelles, publié en 1636 |
Données :
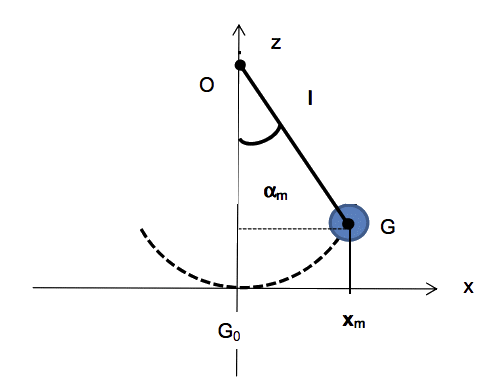
On réalise un pendule en suspendant une bille de plomb de masse m = 50 g et de centre d’inertie G, à un fil de longueur l accroché en O comme l’indique la figure du document 2.
|
|
Document 2
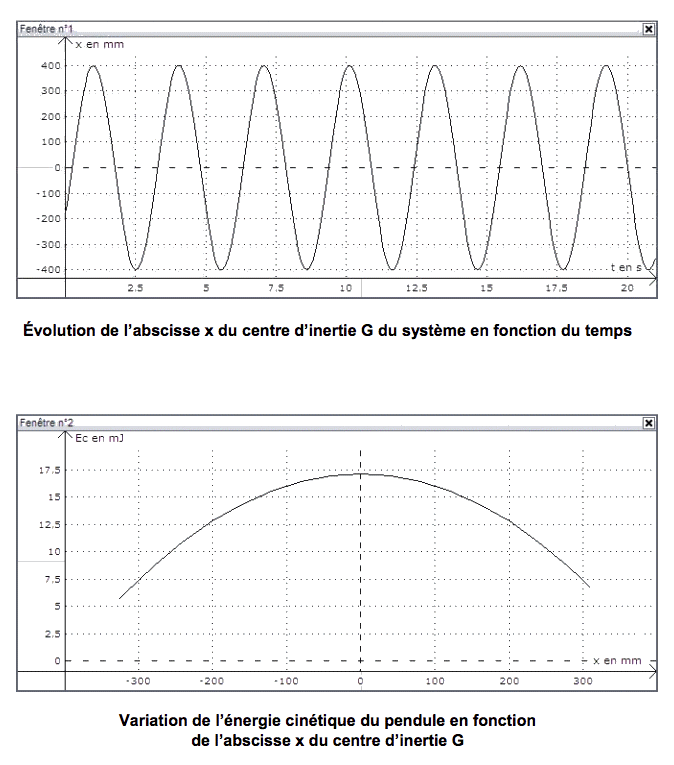
On choisit la position à l’équilibre G0 de G comme origine des altitudes z. Pour un amortissement faible, la pseudo-période T du pendule est voisine de sa période propre T0. L’expression de la période propre du pendule est l’une des propositions suivantes :
|
|
1.1. À l’aide des documents et de vos connaissances, proposer une réponse argumentée pour montrer que « le pendule réalisé aurait pu être celui de Galilée ! ».
|
|
Document
Avec l’horloge atomique – conçue à partir des années 1950/60 – la mesure du temps bascule dans le temps de l’infiniment petit. Ce ne sont plus les oscillations régulières d’un pendule ou d’un ressort spiral qui donnent le rythme à l’horloge. Ici, ce sont les vibrations extrêmement rapides d’une molécule ou d’atome que l’homme a su mettre au profit de la mesure du temps.
D’après L'horloge atomique |
|
2.1. Quelle est la période de retournement de la molécule d’ammoniac ?
NH3 (aq)+ H3O+(aq) ⇆ NH4+(aq) + H2O(ℓ)
Recopier l’équation ci-dessus et expliquer la formation de l’ion ammonium NH4+.
|
| Annexe | |
|
Document 3
| |