Carnet de bac
Annales
Un catalyseur enzymatique, l'uréase |
|
| Métropole 2013 - Exercice 1 - 5 points |
|
L’uréase est une enzyme découverte par J-B Summer en 1926. Elle joue un rôle important au sein des organismes vivants dans la décomposition d’une molécule organique, l’urée. On trouve l’uréase dans des organismes végétaux (comme le haricot sabre) mais également dans des bactéries pathogènes (telles que Helicobacter pylori).
|
|
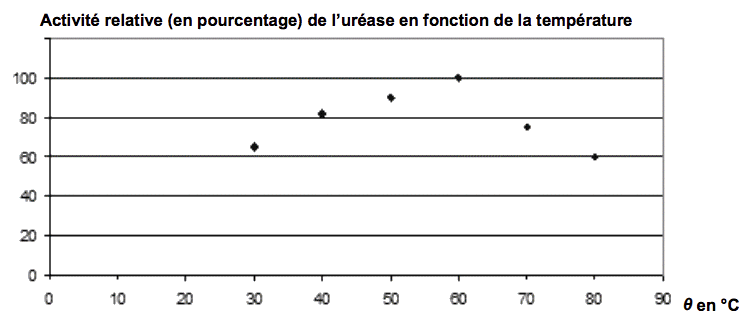
Document 1. Influence de la température sur l’activité enzymatique
La cinétique de la réaction catalysée est directement liée à l’activité de l’uréase : plus l’activité est grande, plus la réaction est rapide. L’activité relative, représentée sur le graphe ci-dessous, est le rapport de l’activité de l’enzyme sur son activité maximale, dans des conditions fixées de température, de pH et pour une quantité d'enzyme donnée.
D’après le site Toyospusa |
|
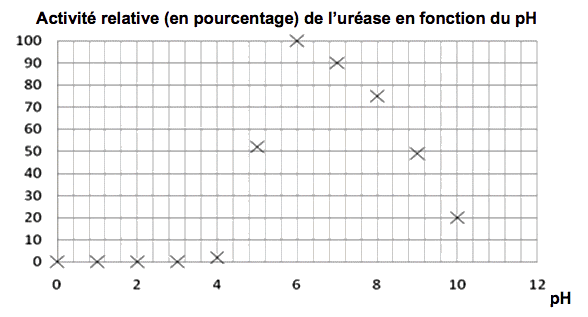
Document 2. Influence du pH sur l’activité enzymatique
Condition expérimentale : température θ = 30°C
D’après le site Toyospusa |
|
1. Activité enzymatique de l’uréase
1.1. L’uréase, un catalyseur
La bactérie Helicobacter pylori (H.pylori) est responsable de la plupart des ulcères de l’estomac chez l’Homme. On souhaite savoir comment elle réussit à survivre dans un milieu très acide, comme l’estomac, en attendant de rejoindre la muqueuse
stomacale où elle pourra se développer. Dans la H.pylori, la réaction de production de l’ammoniac à partir de l’urée se fait selon le processus présenté dans la première partie « Activité enzymatique de l’uréase ».
NH3 (aq)+ H3O+(aq) ⇆ NH4+(aq) + H2O(ℓ)
Quelle est la conséquence de la sécrétion d’ammoniac par la bactérie sur le pH de la solution autour d’elle ?
|